华中科技大学讯 2月20日,自噬领域国际顶级期刊Autophagy发表同济医学院附属梨园医院内分泌科、血管衰老教育部重点实验室金肆教授团队的一项研究,题为“Expression of IMD-CBM peptide induces the autophagic degradation of CAV1 (caveolin 1) to inhibit LDL transcytosis and retard diabetic atherosclerosis”研究论文。
该研究系统揭示了“高血糖 → 自噬抑制 → 小窝蛋白CAV1积累 → LDL跨内皮转运增加 → 动脉粥样硬化加速”的完整分子通路,通过设计一种新型多肽 IMD-CBM,并证实了表达该融合肽通过靶向诱导CAV1选择性自噬降解来干预糖尿病血管并发症的新策略。相关成果已申请国家发明专利。

近年来。我国糖尿病及其并发症的患病率不断攀升,严重影响患病人群的健康状态与预期寿命,其中动脉粥样硬化性心血管疾病(ASCVD)是引起糖尿病患者致死致残最主要原因。在其起始阶段,低密度脂蛋白(LDL)必须穿过完整的内皮屏障才能在内皮下沉积。由于LDL粒径较大,这一过程主要依赖细胞膜上称为“小窝”的特化结构介导的穿胞作用。小窝蛋白-1(CAV1)是形成小窝的关键骨架蛋白,其表达水平直接影响LDL的转运效率。
自噬是细胞清除错误折叠蛋白和受损细胞器的核心稳态机制,曾获得2016年诺贝尔生理学或医学奖,也被认为是解决代谢低下等疾病问题的关键路径。前期研究发现,CAV1与自噬关键蛋白LC3B之间存在相互作用:CAV1的支架结构域(CSD)与LC3B结合会抑制自噬,而其膜内结构域(IMD)与LC3B结合则可促进自噬。在生理状态下,位于膜内的IMD难以接触LC3B,使得CAV1得以稳定存在于膜上并形成小窝。而在高糖环境下,细胞自噬普遍受到抑制,可导致CAV1降解受阻、小窝数量异常增加,进而促进LDL转运与动脉粥样硬化。
基于此,该团队提出一个关键科学问题:能否设计一种“分子桥接工具”,特异性引导CAV1进入自噬降解途径,从而抑制LDL穿胞并延缓糖尿病动脉粥样硬化?
研究团队巧妙地利用CAV1与LC3B的相互作用域,将CAV1中可激活自噬的IMD片段与LC3B中可结合CAV1的CBM(CAV1结合基序)片段连接,构建了一种融合多肽——IMD-CBM。其作用机制为:CBM 与CAV1的CSD结合,竞争性阻断内源性LC3B与CSD的结合(抑制自噬的作用)。IMD 与LC3B结合,主动激活自噬信号。两者协同形成 LC3B-IMD-CBM-CAV1复合物,将CAV1“拉入”自噬途径进行选择性降解。该多肽通过腺病毒载体系统在细胞(HUVECs)和小鼠体内实现高效表达。

IMD-CBM融合肽激活CAV1自噬性降解抑制LDL穿胞机制模式图
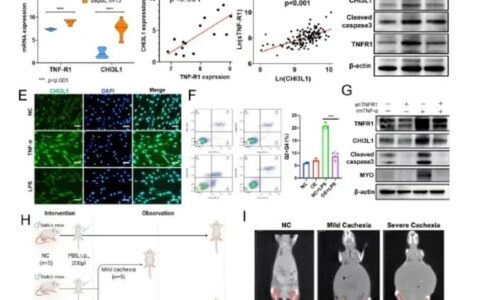
通过LDL穿胞实验发现,在高糖条件下,内皮细胞的LDL穿胞量显著增加;而转染 Ad-IMD-CBM 后,这一过程被显著抑制。采用DiI-LDL标记,共聚焦显微镜观察发现,高糖促进内皮细胞对LDL的摄取,而IMD-CBM处理可明显减少细胞内的LDL荧光信号。提示IMD-CBM能够在高糖环境中逆转LDL的跨内皮转运与细胞内积累。免疫共沉淀与免疫荧光共定位证实,IMD-CBM能够同时与CAV1和LC3B结合。IMD-CBM处理显著降低CAV1蛋白水平。蛋白质半衰期检测发现,CAV1的半衰期从约8.4小时缩短至4.8小时。免疫电镜定位观察显示,IMD-CBM促进CAV1在自噬溶酶体中聚集;共聚焦显微镜观察GFP-CAV1与溶酶体探针共定位增加,表明IMD-CBM确实将CAV1导向了自噬-溶酶体降解途径。超微透射电镜观察到,IMD-CBM处理组细胞中自噬体/自噬溶酶体数量增多,而细胞膜上的小窝数量减少。自噬流检测显示自噬底物p62减少,自噬标记LC3B-II增加。使用溶酶体抑制剂巴佛洛霉素A1后,IMD-CBM处理组的自噬流增强效应更为明显。双标荧光采用GFP-RFP-LC3腺病毒证实,IMD-CBM能增加自噬体与溶酶体融合,表明其提升了完整的自噬通量。在apoe-/-小鼠中,通过建立糖尿病模型,并喂养高脂饮食构建动脉粥样硬化模型。通过尾静脉注射内皮细胞特异性表达IMD-CBM的腺病毒。斑块分析显示主动脉整体油红O染色及主动脉根部切片显示,IMD-CBM治疗显著减少了糖尿病小鼠的动脉粥样硬化斑块面积。小鼠主动脉免疫荧光显示IMD-CBM与CAV1/LC3B共定位;免疫组化显示治疗组CAV1和p62表达下降,LC3B表达上升;透射电镜同样观察到小窝减少、自噬结构增加。IMD-CBM治疗还降低了糖尿病小鼠的血清甘油三酯(TG)、总胆固醇(CHO)及血糖水平。
该研究从临床难题出发,深入分子细胞机制,成功设计出一种具有生物学功能的全新多肽分子,并在细胞和动物模型中系统验证了其治疗潜能。它不仅揭示了糖尿病加速动脉粥样硬化的一个关键环节,更展示了一种“靶向自噬降解”的治疗新范式。IMD-CBM作为一种新的分子干预策略,为糖尿病动脉粥样硬化的治疗提供了潜在的候选药物前体。它提示,未来药物研发可着眼于调控内皮细胞自噬或特异性降解CAV1,从而在降脂之外,更直接地对抗高血糖导致的血管损伤。未来,进一步优化IMD-CBM的递送方式并探索其与其他代谢调控药物的联用效果,将推动该策略向临床转化迈出更坚实的步伐。
金肆为通讯作者。博士生王力为第一作者,博士生贾雄、柏湘利、赵颖、程文卓、舒梦、舒妍、张力引、王若楠等参与了相关工作。华中科技大学为第一完成单位和通讯作者单位。本研究得到了国家重点研发计划、国家自然科学基金和湖北省医学领军人才基金等项目的资助和支持。
原文链接:https://www.tandfonline.com/doi/10.1080/15548627.2026.2631946
原创文章,作者:荆楚之窗,如若转载,请注明出处:https://www.jingchucn.com/92720/