
华中农业大学讯(通讯员 陶大刚)近日,动物科学技术学院、动物医学院猪基因组与育种团队联合崖州湾国家实验室等单位研究成果以“Structural mining and engineering of metagenome-derived Cas12a orthologs expands the CRISPR genome editing and multiplex diagnostics toolkit”为题在Molecular Therapy发表。
研究通过蛋白结构聚类与工程化改造策略,从宏基因组大数据中挖掘并优化获得一种兼具高编辑活性与强特异性的新型Cas12a变体——PcuCas12a MAX(亦称Gs12-7MAX),展现出优异的基因组编辑性能。同时,研究团队还鉴定出四种具有不同单链DNA反式切割活性的Cas12a变体(LcoCas12a、FcaCas12a、EsoCas12a和Mac2Cas12a),进一步拓展了CRISPR工具的功能多样性。基于上述发现,研究建立了高效高保真的PcuCas12a MAX基因组编辑系统,并开发出适用于多重CRISPR核酸检测的新技术平台。该研究为基因组编辑工具的开发与应用提供了新思路,在基础科学研究、动植物与水产育种、核酸检测及基因治疗等领域具有广阔的应用前景。
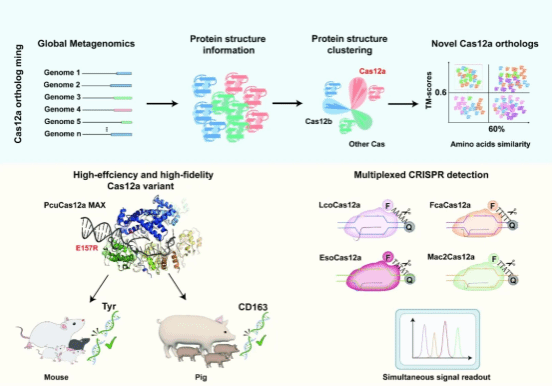
CRISPR-Cas12a作为一种结构紧凑的RNA引导核酸酶,已在基因组编辑和分子诊断领域得到广泛应用。然而,其顺式切割效率仍有提升空间,反式切割特性亦尚未完全阐明,限制了该工具的进一步拓展。为突破这些瓶颈,研究团队采用蛋白结构聚类与工程化改造相结合的策略,从海量微生物宏基因组数据中成功识别出多个此前未被表征的Cas12a家族新成员。通过系统筛选出21种蛋白结构保守但氨基酸序列高度分化的候选蛋白,并系统评估其顺式与反式切割活性,最终获得一系列功能特性多样化的基因编辑新工具。
一是高保真PcuCas12a MAX,可实现多物种高效精准基因组编辑。通过比较顺式切割活性,研究团队发现PcuCas12a在候选蛋白中具有最高的核酸内切酶活性。在此基础上,结合结构预测指导的蛋白质工程化改造,成功构建了高保真变体PcuCas12a MAX。活性评估结果显示,PcuCas12a MAX在HEK293T细胞中的平均编辑效率与已知高活性变体AsCas12a Ultra相当,而GUIDE-Seq全基因组脱靶分析进一步表明,其编辑特异性显著优于后者。
研究重点评估了PcuCas12a MAX的跨物种基因组编辑能力。在小鼠模型中,针对Tyr基因的胚胎显微注射高效获得了白化表型F0代小鼠,验证了该工具在制备基因编辑动物模型中的高效性。此外,研究团队已成功利用该工具制备出CD163基因敲除的抗蓝耳病猪育种新材料,为抗病育种研究提供了重要技术支撑。
二是反式切割活性特异的Cas12a新变体,助力实现CRISPR多重核酸检测。通过比较反式切割活性,研究团队发现LcoCas12a、FcaCas12a、EsoCas12a和Mac2Cas12a四种新型Cas12a同源物,在与工程化改造的CRISPR RNA配对后,展现出独特的单链DNA反式切割特征。基于这一特性,团队成功构建了可同时检测多种核酸靶标的多重CRISPR传感器平台。该研究显著丰富了Cas12a核酸检测工具库,拓展了其在下一代分子诊断中的应用潜力。
华中农业大学博士后陶大刚与刘海龙、在读博士生李晟,以及崖州湾国家实验室在读博士生徐兵荣为该论文的共同第一作者。崖州湾国家实验室赵书红教授、华中农业大学动物科学技术学院、动物医学院李新云教授和谢胜松教授为该论文的共同通讯作者。西北农林科技大学魏迎辉教授、崖州湾国家实验室赵长志主任科学家、浙江大学医学院附属第一医院黄行许教授等对该研究提供了重要指导和帮助。
审核人:李新云
【英文摘要】
CRISPR-Cas12a is a compact, RNA-guided nuclease widely deployed in genome editing and molecular diagnostics, yet its broader utility is limited by suboptimal cis-cleavage efficiency and incompletely defined trans-cleavage behavior. To overcome these constraints, we developed an Artificial Intelligence (AI)-guided structural discovery pipeline powered by AlphaFold2, which identified 1,261 previously uncharacterized Cas12a orthologs. From this set, 21 structurally conserved but sequence-divergent candidates were selected for biochemical characterization. Using structure-informed engineering, we generated PcuCas12a MAX, a high-fidelity variant that achieves genome-editing efficiencies in human cells comparable to the benchmark AsCas12a Ultra, while retaining robust activity in murine and porcine systems. In addition, four orthologs (LcoCas12a, FcaCas12a, EsoCas12a, and Mac2Cas12a), when paired with specifically engineered CRISPR RNAs, exhibited distinct single-stranded DNA trans-cleavage signatures. These properties enabled construction of a multiplex CRISPR sensor capable of simultaneously detecting multiple nucleic acid targets. Together, these findings expand the Cas12a endonuclease repertoire and enhance its utility in genome engineering and next-generation diagnostics.
论文链接:https://www.sciencedirect.com/science/article/pii/S1525001626001966
原创文章,作者:荆楚之窗,如若转载,请注明出处:https://www.jingchucn.com/92676/













